I. LÝ THUYẾT
1) Nguyên tắc
– Phải trích mỗi chất một ít để làm mẫu thử ( trừ trường hợp là chất khí )
– Phản ứng chọn để nhận biết các chất phải xảy ra nhanh và có dấu hiệu đặc trưng ( đổi màu , xuất hiện kết tủa, sủi bọt khí, mùi đặc trưng, … )
2) Phương pháp
– Phân loại các chất mất nhãn → xác định tính chất đặc trưng → chọn thuốc thử.
– Trình bày :
Nêu thuốc thử đã chọn ? Chất đã nhận ra ? Dấu hiệu nhận biết (Hiện tượng gì ? ), viết PTHH xảy ra để minh hoạ cho các hiện tượng.
3) Lưu ý
– Nếu chất A là thuốc thử của chất B thì chất B cũng là thuốc thử của A.
– Nếu chỉ được lấy thêm 1 thuốc thử, thì chất lấy vào phải nhận ra được một chất sao cho chất này có khả năng làm thuốc thử cho các chất còn lại.
– Nếu không dùng thuốc thử thì dùng các phản ứng phân hủy, hoặc cho tác dụng đôi một.
– Khi chứng minh sự có mặt của một chất trong hỗn hợp thì rất dễ nhầm lẫn. Vì vậy thuốc thử được dùng phải rất đặc trưng.
Ví dụ: Không thể dùng nước vôi trong để chứng minh sự có mặt của CO2 trong hỗn hợp : CO2, SO2, NH3 vì SO2 cũng làm đục nước vôi trong:
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O
4) Tóm tắt thuốc thử và dấu hiệu nhận biết một số chất
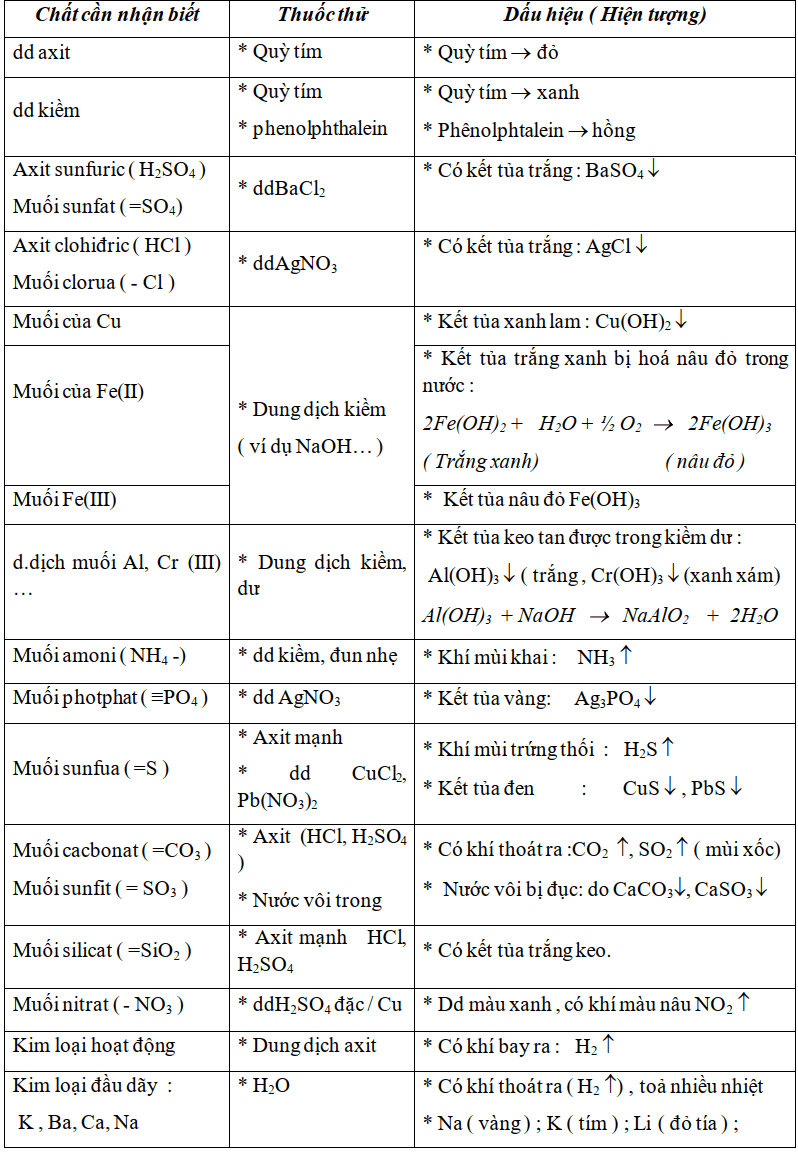
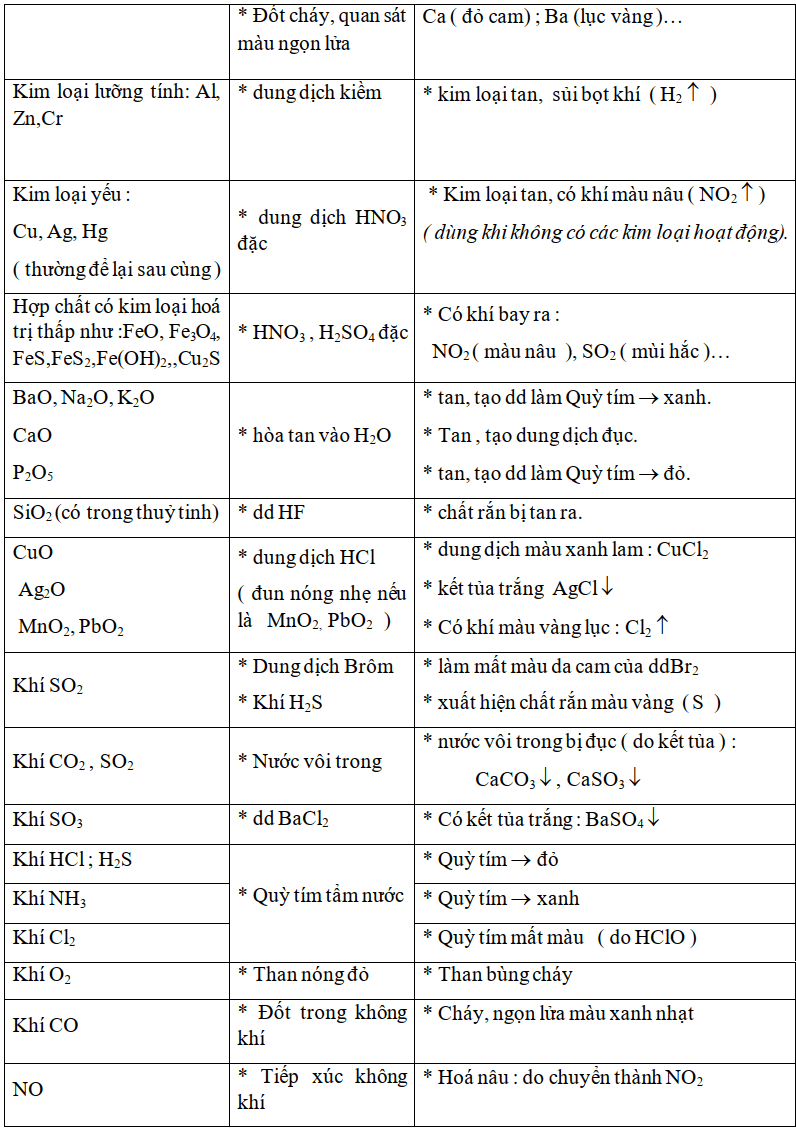
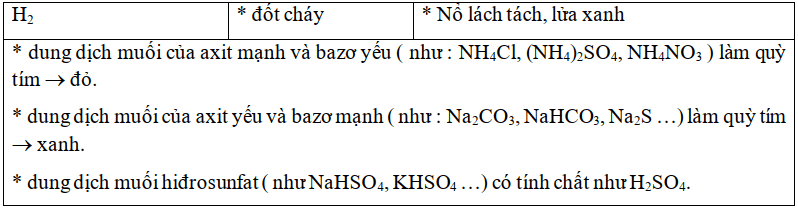
II. BÀI TẬP MẪU



III. BÀI TẬP ÁP DỤNG
Dạng 1: Không hạn chế thuốc thử
Oxit
1. K2O, Al2O3, MgO
2. K2O, Al2O3, CaO
3. Ag2O , Fe2O3, CuO, Fe3O4 và FeO
4. Na2O, Al2O3, Fe2O3 và Fe
5. Fe3O4 và Fe2O3
6. Hỗn hợp ( Al + Al2O3 ), ( Fe + Fe2O3 ) và ( FeO + Fe2O3 )
Muối
1. Dung dịch AlCl3, NH4NO3, BaCl2 và MgCl2
2. Dung dịch NaOH, H2SO4, Na2SO4, BaCl2 và MgCl2
3. Dung dịch FeCl3, Al(NO3)3 , HCl, NH4NO3, KOH và Pb(NO3)2
Dạng 2: Chỉ dùng một loại hoá chất
Kim loại
1. Zn, Fe và Ba
2. Ba, Mg, Fe, Ag và Al mà chỉ dùng H2SO4
Oxit
1. Na2O, Al2O3 và Fe2O3
2. K2O, Al2O3, CaO và MgO
Muối
1. Dung dịch BaCl2, Fe(NO3)2, AgNO3 và Na2CO3
2. Chất rắn NaCl, Na2CO3, BaCO3, BaSO4
3. Chỉ dùng CO2 và H2O phân biệt dung dịch NaCl, Na2SO4, CaCO3, Na2CO3 và BaSO4
4. Chỉ dùng kim loại phân biệt dung dịch HCl, HNO3đ, NaNO3, NaOH, AgNO3
5. Chỉ dùng HCl và H2O phân biệt các chất rắn Na2CO3, CaCO3, Na2SO4 và CaSO4.2H2O
6. Dung dịch NH4HSO4, Ba(OH)2, BaCl2, HCl, NaCl, H2SO4
7. Dùng quỳ tím phân biệt dung dịch H2SO4, Ba(OH)2, BaCl2, HCl, NaCl, NaOH
8. Chỉ dùng CO2 và H2O phân biệt các chất rắn NaCl, Na2CO3, CaCO3 và BaSO4
9. Chỉ dùng kim loại phân biệt dung dịch AgNO3, NaOH, HCl, NaNO3
10. Dung dịch BaCl2, Na2SO4, Na3PO4, HNO3
11. Dung dịch H2SO4, Na2SO4, Na2CO3, FeSO4
Dạng 3:
Không dùng thuốc thử nào khác hãy phân biệt các dung dịch không màu sau :
1. HCl, MgSO4, NaOH, BaCl2, NaCl
2. NaCl, NaOH, HCl, phenolphthalein
3. K2SO4, Al(NO3)3, NH4(SO4)2, Ba(NO3)2, NaOH
*Download file word Bảng nhận biết các chất hóa học lớp 8, lớp 9.docx bằng cách click vào nút Tải về dưới đây.

